Применение РНК препаратов в лечении редких заболеваний становится одним из ключевых направлений современной биомедицины, открывая новые возможности для воздействия на молекулярные причины заболеваний.
В мире известно более 7000 редких заболеваний, из которых свыше 80% имеют моногенную природу. Общее число пациентов превышает 300 миллионов человек, однако эффективные методы лечения разработаны менее чем для 5% нозологий.
👉 На протяжении длительного периода традиционные маломолекулярные лекарства, антителные лекарства и ферментативная заместительнаятерапия страдали от ограничений в отношении мишеней, высокой частоты введения, высокой стоимости и других проблем, не сумев достигнуть корня генетических заболеваний — дефицита белка или накопления токсических белков, вызванных нарушением экспрессии генов.
Возникновение РНК-препаратов постепенно меняет эту ситуацию. Как новое поколение биологической терапии с точным таргетированием экспрессии генов, РНК-препараты могут обеспечить точную регуляцию патогенных генов и восстановление функциональных белков на посттранскрипционном уровне без изменения геномной ДНК.
Они естественным образом соответствуют ключевой характеристике редких генетических заболеваний — «моногенное патогенез», и становятся важным технологическим путем для преодоления «нелечимых» заболеваний.
В этом процессе, помимо инноваций в верхней части цепочки разработки, доступность лекарств и система их снабжения также имеют решающее значение. 🔻
Фармацевтические распределительные предприятия, среди которых выделяется DengYue Medicine, играют ключевую роль в соединении инновационных методов лечения с пациентами за счет интеграции глобальных ресурсов лекарств и строительства законных каналов снабжения, способствуя более эффективному внедрению передовых методов лечения, включая РНК-препараты, в клинические сценарии применения.
В данной статье рассматривается применение РНК препаратов в лечении редких заболеваний, анализируются их ключевые механизмы действия, обобщаются достижения в клиническом внедрении и оценивается влияние этих технологий на трансформацию подходов к диагностике и терапии редких заболеваний.
Ключевой механизм действия РНК-препаратов: точное вмешательство в экспрессию генов, направленное на корень редких заболеваний
Большинство редких генетических заболеваний по своей сути являются цепными реакциями, вызванными мутациями генов: либо происходит ошибка в процессе транскрипции и сплайсинга мРНК, либо синтезируются нефункциональные или токсические белки, которые в конечном итоге повреждают органы и вызывают заболевания.
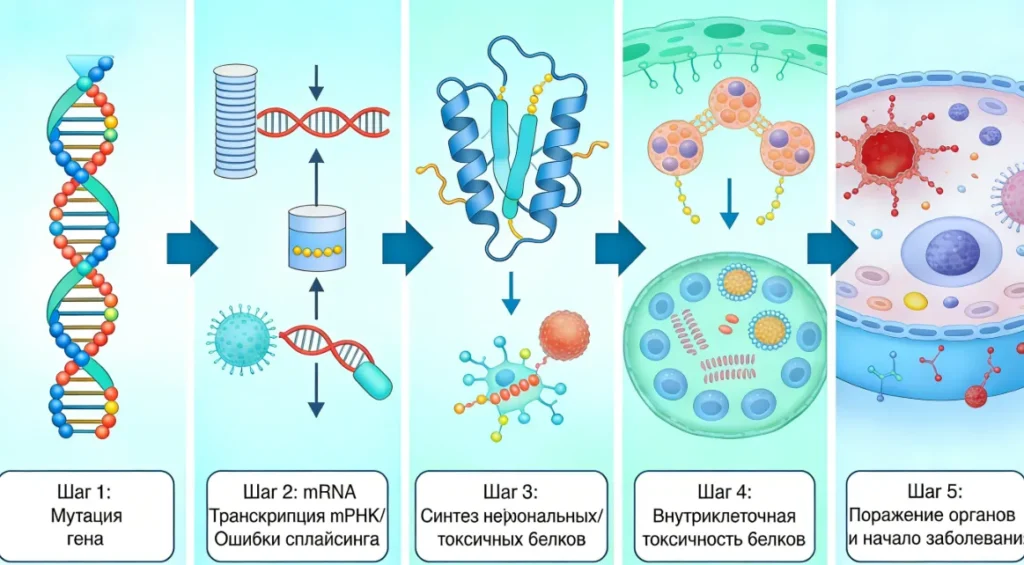
РНК-препараты, опираясь на принцип комплементарности нуклеиновых кислот, точно вмешиваются в жизненный цикл РНК в клетках и могут достичь трех ключевых целей лечения без изменения генома: подавление патогенных генов, восстановление функциональных белков и дополнение отсутствующих белков. Их безопасность и таргетичность значительно превосходят традиционные методы лечения.
1. Антисмысловые олигонуклеотиды (АСО): коррекция сплайсинга и деградация патогенной мРНК — наиболее зрелый класс РНК-терапии
Антисмысловые олигонуклеотиды (АСО) представляют собой химически модифицированные короткие одноцепочечные нуклеиновые кислоты, обладающие высокой стабильностью и специфичностью к мишени.
‼️ Это один из первых классов РНК-препаратов, одобренных для лечения редких генетических заболеваний.
Механизм их действия реализуется по двум основным направлениям.
- Во-первых, АСО рекрутируют эндогенный фермент RNase H, который селективно расщепляет комплементарную патологическую мРНК, предотвращая синтез токсичных белков.
- Во-вторых, они способны модифицировать процесс сплайсинга пре-мРНК за счёт стерического блокирования регуляторных участков, способствуя восстановлению синтеза функциональных белков.
Данный подход особенно эффективен при неврологических редких заболеваниях, таких как спинальная мышечная атрофия (СМА), боковой амиотрофический склероз (БАС), синдром Драве и др. АСО характеризуются высокой специфичностью и низким риском офф-таргет эффектов.
💉 Возможность локального введения (включая интратекальное и подкожное) обеспечивает высокую точность доставки, что делает их важным инструментом терапии заболеваний центральной нервной системы.
2. Малые интерферирующие РНК (siRNA): высокоэффективное и длительное подавление экспрессии генов — оптимальное решение для заболеваний печени
Малые интерферирующие РНК (siRNA) представляют собой короткие двуцепочечные молекулы РНК, которые после проникновения в клетку интегрируются в RISC-комплекс и направляют его на специфическое расщепление комплементарной мРНК, обеспечивая почти полное подавление экспрессии целевого гена.
В сочетании с технологиями направленной доставки в печень, такими как GalNAc-конъюгация, siRNA-препараты способны селективно накапливаться в гепатоцитах. При этом терапевтический эффект после однократного введения может сохраняться в течение нескольких месяцев, что существенно снижает частоту дозирования и делает данный подход особенно эффективным при длительном лечении метаболических и амилоидных редких заболеваний.
По сравнению с АСО, siRNA характеризуются более высокой эффективностью подавления и требуют меньших доз.
Они демонстрируют значительные преимущества при заболеваниях печени, таких как наследственный транстиретиновый амилоидоз (hATTR) и семейная хиломикронемия, а также способствуют повышению приверженности пациентов терапии.
3. мРНК-терапия: внутриклеточный синтез функциональных белков — решение проблемы ферментных дефицитов
Концепция мРНК-терапии основана на доставке в клетки синтетически полученной и модифицированной мРНК, которая функционирует как матрица для синтеза белка, направляя рибосомы на продукцию функциональных белков, отсутствующих или дефицитных в организме.
👉 По сравнению с традиционной генной терапией, мРНК не интегрируется в геном, не несёт риска инсерционных мутаций, а её экспрессия является временной и контролируемой, что обеспечивает более высокий профиль безопасности.
👉 В отличие от ферментозаместительной терапии, мРНК обеспечивает синтез белков непосредственно внутри клеток (in situ), что повышает биодоступность и потенциально снижает долгосрочную нагрузку на систему лечения.
В настоящее время мРНК-терапия активно развивается в области лечения редких генетических заболеваний, связанных с ферментными дефицитами, включая кистозный фиброз и лизосомные болезни накопления. Ряд препаратов уже находится на средних и поздних стадиях клинических исследований.
4. Технологии редактирования РНК: точечная коррекция мутаций — новый подход к лечению моногенных заболеваний
Новое поколение технологий редактирования РНК, включая системы на основе ADAR и платформы AIM, использует эндогенные ферментные механизмы для точечной модификации нуклеотидов мРНК и коррекции ошибок сплайсинга без вмешательства в ДНК.
Данный подход позволяет преодолеть ограничения традиционных РНК-препаратов, которые не способны исправлять точечные мутации. Технологии редактирования РНК обладают обратимостью, регулируемостью и низким уровнем офф-таргет эффектов.
Они открывают новые возможности для лечения редких заболеваний, вызванных однонуклеотидными мутациями, включая серповидноклеточную анемию, болезнь Фабри и наследственные заболевания сетчатки.
🧑⚕️ 💡От зрелых технологий АСО и siRNA до развивающейся мРНК-терапии и передовых методов редактирования РНК — РНК-препараты формируют комплексную терапевтическую платформу, охватывающую различные механизмы патогенеза редких заболеваний.
Эти высокоточные и эффективные подходы уже демонстрируют значимые клинические результаты и постепенно трансформируют парадигму лечения редких заболеваний.
Прогресс в внедрении РНК-препаратов: от одобрения к расширению конвейера, изменение истории лечения редких заболеваний
Благодаря уникальным преимуществам механизма РНК-препараты стали ключевым направлением в разработке лекарств для редких заболеваний.
По всему миру несколько лекарств успешно одобрены к применению, а большое количество препаратов в стадии разработки продвинуто до клинических испытаний, охватывая нейрологические, метаболические, офтальмологические, гематологические и другие области заболеваний, полностью разбивая индустриальный обряд «редкие заболевания нелечимы».
1️⃣ Одобренные препараты: формирование нового стандарта прецизионной терапии редких заболеваний
- Спинальная мышечная атрофия (СМА):
Nusinersen (АСО) — первый в мире препарат, направленно воздействующий на СМА.
Он модулирует сплайсинг гена SMN2, восстанавливая экспрессию функционального белка SMN, что значительно повышает выживаемость пациентов и радикально изменило естественное течение заболевания.
- Наследственный транстиретиновый амилоидоз (hATTR):
Patisiran и Vutrisiran (siRNA) обеспечивают длительное подавление экспрессии гена TTR.
Клинические исследования демонстрируют снижение уровня патогенного белка более чем на 80%, что сопровождается замедлением нейропатических и кардиальных проявлений. Подкожное введение с интервалом до 3 месяцев обеспечивает устойчивый терапевтический эффект.
- Боковой амиотрофический склероз (БАС):
Tofersen (АСО) селективно подавляет экспрессию мутантного гена SOD1 и является первым одобренным препаратом, направленным на патогенетическое лечение данной формы БАС.
- Семейная хиломикронемия:
Volanesorsen (АСО) и siRNA-препараты (например, Olezarsen) ингибируют синтез аполипопротеина C-III, снижая уровень триглицеридов более чем на 70–80% и существенно уменьшая риск острого панкреатита.
- Синдром Драве:
Zorevunersen (АСО) направлен на повышение экспрессии гена SCN1A, что способствует увеличению уровня функционального белка и ассоциировано со снижением частоты судорожных приступов и улучшением нейрокогнитивных функций.
2️⃣ Перспективный pipeline: расширение границ терапии редких заболеваний
Глобальный pipeline РНК-препаратов для лечения редких заболеваний продолжает активно расширяться. Ряд кандидатов уже достиг поздних стадий клинических исследований, охватывая ранее трудно поддающиеся терапии нозологии:
- Нейромышечные заболевания: конъюгированные siRNA-препараты, направленные на DUX4 при фасциоскапулогумеральной мышечной дистрофии (FSHD), демонстрируют значимое улучшение мышечной функции в доклинических моделях.
- Лизосомные болезни накопления: АСО-терапия способна корректировать нарушения сплайсинга при болезни Фабри; разрабатываются также подходы, направленные на преодоление гематоэнцефалического барьера.
- Офтальмологические редкие заболевания: технологии редактирования РНК позволяют непосредственно корректировать мутации в клетках сетчатки при интравитреальном введении; в ранних клинических исследованиях отмечено улучшение зрительных функций у части пациентов.
- Болезнь Хантингтона: АСО- и siRNA-препараты, направленные на ген HTT, демонстрируют устойчивое снижение уровня мутантного белка и потенциал замедления прогрессирования заболевания.
3️⃣ Технологические инновации: оптимизация доставки и молекулярного дизайна
Быстрое развитие технологий существенно расширяет клинический потенциал РНК-препаратов:
- Новые подходы, включая редактирование РНК и технологии подавления преждевременных стоп-кодонов (read-through), открывают возможности для лечения заболеваний, ранее недоступных для таргетной терапии.
- GalNAc-конъюгация обеспечивает высокоэффективную адресную доставку в гепатоциты;
- Липидные наночастицы (LNP) повышают эффективность доставки в ткани центральной нервной системы и органы зрения;
- Химические модификации (например, фосфоротиоатные связи, 2′-O-MOE) увеличивают стабильность молекул и снижают иммуногенность;
🔬 Как яркие клинические результаты одобренных препаратов, так и широкие перспективы препаратов в стадии разработки в конечном счете обусловлены ключевыми преимуществами РНК-препаратов по сравнению с традиционными методами лечения, что и является ключевой причиной их превосходства в лечении редких заболеваний.
Ключевые преимущества РНК-препаратов: почему они становятся предпочтительным направлением в лечении редких заболеваний?
✅ Прецизионное таргетирование: воздействие на молекулярную причину заболевания
Благодаря принципу комплементарности нуклеиновых кислот, РНК-препараты способны селективно распознавать и воздействовать на патогенные РНК, минимально влияя на экспрессию нормальных генов. Это делает их особенно эффективными для терапии моногенных наследственных заболеваний.
Кроме того, РНК-терапия открывает возможности для воздействия на так называемые «недоступные» мишени, которые трудно или невозможно таргетировать с помощью малых молекул или моноклональных антител.
✅ Безопасность и управляемость: отсутствие геномной интеграции
РНК-препараты реализуют своё действие преимущественно на уровне РНК и, как правило, не интегрируются в геномную ДНК, что позволяет избежать рисков, связанных с инсерционными мутациями, характерными для некоторых подходов генной терапии.
Терапевтический эффект РНК-препаратов является дозозависимым и, как правило, обратимым, что обеспечивает возможность гибкой коррекции лечения в зависимости от клинического ответа пациента. В совокупности это формирует благоприятный профиль безопасности по сравнению с ДНК-ориентированными технологиями.
✅ Эффективность разработки и доступность
Разработка РНК-препаратов основана преимущественно на дизайне нуклеотидной последовательности и химическом синтезе, что позволяет избежать сложных этапов белковой экспрессии и очистки и существенно сокращает сроки вывода препаратов в клинику.
Гибкость платформы даёт возможность оперативно адаптировать последовательности под различные мутационные варианты, способствуя развитию персонализированной терапии.
Кроме того, пролонгированные формы siRNA позволяют снизить частоту введения до одного раза в несколько месяцев, что повышает приверженность пациентов лечению и потенциально снижает долгосрочную экономическую нагрузку.
🤔Несмотря на значительные преимущества и уже достигнутые клинические результаты, РНК-препараты по-прежнему сталкиваются с рядом технологических и практических ограничений.
Ключевыми направлениями дальнейшего развития остаются оптимизация систем доставки, повышение тканевой специфичности, снижение иммуногенности и расширение спектра показаний, включая более сложные и редкие формы заболеваний.
Будущее развитие
С учётом текущего уровня клинического применения, дальнейшее расширение применения РНК препаратов в лечении редких заболеваний и повышение их доступности для пациентов по-прежнему сопряжены с рядом ключевых вызовов, включая эффективность доставки, иммуногенность, проницаемость через гематоэнцефалический барьер и долгосрочную безопасность.
В ответ на эти ограничения отрасль в ближайшие годы сосредоточится на трёх приоритетных направлениях:
- Совершенствование технологий доставки: разработка новых систем таргетированной доставки в центральную нервную систему, мышечные ткани и органы зрения, что позволит значительно расширить применение РНК препаратов в лечении редких заболеваний за пределами текущих показаний;
- Ускорение трансляции передовых технологий: внедрение таких подходов, как редактирование РНК, технологии read-through и циркулярные РНК, открывает новые возможности для дальнейшего развития применения РНК препаратов в лечении редких заболеваний, особенно при однонуклеотидных и нонсенс-мутациях;
- Развитие персонализированной и доступной терапии: индивидуализация лечения и оптимизация производства будут способствовать более широкому применению РНК препаратов в лечении редких заболеваний в клинической практике.
РНК-препараты, благодаря своему уникальному механизму действия, уже существенно трансформировали подход к лечению редких генетических заболеваний и стали основой для расширения применения РНК препаратов в лечении редких заболеваний на практике.
✨ По мере дальнейшего технологического прогресса и расширения клинического pipeline, применение РНК препаратов в лечении редких заболеваний будет продолжать расти, формируя новую парадигму терапии и обеспечивая пациентам доступ к более точным и эффективным методам лечения.
FAQ: Применение РНК препаратов в лечении редких заболеваний
Что такое лекарства на основе РНК?
Эти препараты представляют собой короткие последовательности РНК, которые присоединяются к мРНК и препятствуют синтезу белка, кодируемого определенным геном.
Антисмысловые препараты разрабатываются для лечения рака легких, диабета и таких заболеваний, как артрит и астма, имеющих выраженный воспалительный компонент.
Что такое РНК-терапия?
РНК—терапия — динамично развивающееся направление современной медицины, основанное на использовании различных типов молекул рибонуклеиновой кислоты для направленной регуляции продукции белков, участвующих в развитии патологий.
Как работает РНК-терапия?
Терапия на основе РНК действует путем манипулирования экспрессией и активностью определенных целевых молекул , предоставляя средства для лечения заболеваний, которые не поддаются лечению традиционными лекарственными препаратами.
Являются ли РНК-терапия биологическими препаратами?
К ним относятся мРНК-вакцины и препараты клеточной и генной терапии (КГТ), в том числе те, которые используют системы доставки вирусных векторов для некоторых видов РНК-терапии.
Они регулируются как биологические лекарственные средства в соответствии с заявкой на получение лицензии на биологический препарат (BLA) .
