В эпоху глубокой трансформации прецизионной медицины биспецифические антитела и синергетический эффект становятся ключевыми темами современного онкологического лечения. Моноклональные антитела когда-то обеспечивали высокую специфичность и низкую токсичность, однако ограниченность терапии с одним таргетом приводит к развитию резистентности и снижает эффективность лечения.
В этом контексте биспецифические антитела (BsAb, Bispecific Antibodies), способные одновременно воздействовать на две мишени, представляют собой инновационную терапию, переопределяющую функциональные возможности антител. Их ключевая ценность заключается не только в «наличии дополнительной мишени», но и в многомерной синергии, обеспечивающей противораковый эффект «1+1>2».
Платформа DengYueMedicine, следящая за передовыми мировыми тенденциями в лечении опухолей, также внимательно отслеживает развитие и клиническую ценность биспецифических антител и других инновационных методов терапии.
Структурная основа двойных специфических антител: фундаментальная логика проектирования «двух мишеней»
Тот факт, что двойные специфические антитела могут обеспечить противоопухолевый эффект «1+1>2», коренится в их уникальном молекулярном дизайне, отличающемся от традиционных моноклональных антител.
Традиционные моноклональные антитела обычно содержат один антиген-связывающий домен и могут распознавать и воздействовать только на один эпитоп антигена. Этот режим «точечного воздействия» обладает хорошей специфичностью к мишени в определенных ситуациях, но часто не может стабильно проявлять эффективность при столкновении с высоко гетерогенной и динамически изменяющейся опухолевой микросредой.
Напротив, двойные специфические антитела с помощью генной инженерии или клеточной инженерии интегрируют два различных антиген-связывающих фрагмента (Fab-фрагмента) в единую молекулярную структуру антитела, благодаря чему могут одновременно распознавать и связываться с двумя различными антигенами или различными эпитопами одного и того же антигена.
Однако значение этого структурного инновационного решения не ограничивается просто «добавлением одной мишени». Более важно, что оно отражает логику синергетического проектирования на функциональном уровне:
- Один конец может точно распознавать специфические маркеры на поверхности опухолевых клеток (например, CD19, HER2, BCMA)
- Другой конец может связываться с активационными рецепторами иммунных клеток (например, Т-лимфоцитов, НК-клеток) (например, CD3, CD16)
- Или одновременно воздействовать на два ключевых опухолевых сигнальных пути, реализуя двойную блокаду
Эта способность «межклеточного» или «межпутевого» соединения интегрирует первоначально независимые биологические процессы в единую функциональную систему, создавая условия для возникновения синергетического эффекта.
Таким образом, структурное проектирование двойных специфических антител по своей сути не является простым «суперпозицией фрагментов», а представляет собой точно оптимизированную платформу функциональной интеграции.
Именно это структурное инновационное решение обеспечивает физическую основу для «синергетического воздействия на несколько мишеней» и создает предпосылки для суперпозиции таких механизмов, как активация иммунитета и усиление сигнала, на последующих этапах.
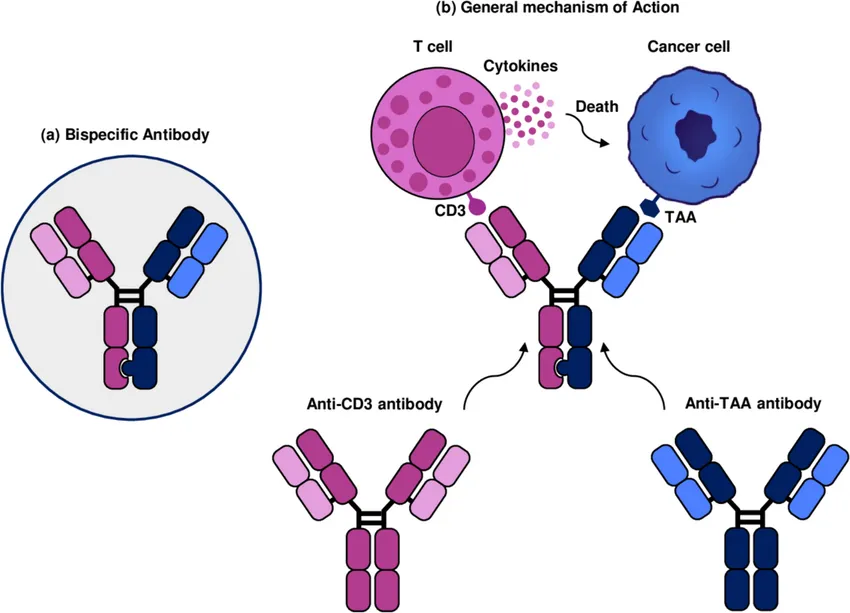
Три основных механизма: создание синергетической системы эффективности «1+1>2»
Основываясь на структуре двух мишеней, двойные специфические антитела развили три классических механизма действия, которые не существуют изолированно, а образуют синергетический эффект на трех уровнях — активация иммунитета, блокада сигнала и высвобождение иммунной функции, совместно обеспечивая значительное повышение терапевтической эффективности.
(I)Механизм клеточного мостикования: от «пассивного распознавания» к «активному направленному уничтожению»
Среди трех механизмов наиболее представительный и наиболее освоенный в клиническом применении — механизм клеточного мостикования (перенаправления Т-лимфоцитов).
Его суть заключается в создании функционального моста «опухолевая клетка — антитело — иммунная клетка»:
Один конец антитела специфически связывается с антигеном на поверхности опухолевой клетки, а другой конец направлен на активационную молекулу на поверхности иммунной клетки (например, CD3 на Т-лимфоцитах).
Благодаря физическому соединению иммунные клетки напрямую направляются к опухолевым клеткам и немедленно запускают цитотоксическую реакцию. В отличие от традиционного способа, основанного на презентации антигена и активации иммунитета, этот механизм позволяет:
- Обойти естественный процесс запуска иммунитета
- Прямо активировать эффекторные Т-лимфоциты
- Быстро индуцировать лизис опухолевых клеток
👉 С точки зрения сути механизма, это преобразование «неопределенности иммунного распознавания» в «определенность направленного контроля».
Поэтому его синергетическое преимущество проявляется прежде всего в следующем:
- Специфичность выше: уничтожение клеток запускается только при одновременной связи с двумя мишенями, снижая риск нецелевого воздействия
- Эффективность выше: значительно увеличивает вероятность контакта и уничтожения опухолевых клеток иммунными клетками
- Применяемость шире: особенно эффективно при опухолях с недостаточной иммунной инфильтрацией
На примере блинатумомаба (Blinatumomab, CD3×CD19) можно видеть, что этот механизм уже доказал свою клиническую ценность в лечении гематологических опухолей.
👉 Этот механизм заложил первый уровень логики эффекта «1+1>2»: синергия пространства и функции.
(II)Двойная блокада сигнальных путей: от «точечного подавления» к «сетевому подавлению»
Если механизм клеточного мостика отвечает на вопрос «как более эффективно уничтожать опухолевые клетки», то второй механизм сосредоточен на следующем:
👉 как предотвратить уклонение опухоли от терапии и развитие лекарственной устойчивости
Опухоли обладают высокой адаптационной способностью, в основе которой лежит сложная сигнальная сеть. При подавлении одного сигнального пути другие пути часто активируются, формируя так называемый «компенсаторный механизм», что является одной из ключевых причин ограниченной эффективности моноклональных антител.
Биспецифические антитела позволяют одновременно воздействовать на:
- два ключевых узла одного и того же сигнального пути
- или две взаимосвязанные онкогенные сигнальные цепи
тем самым обеспечивая двойную блокаду сигналов, поддерживающих выживание опухоли.
На примере немелкоклеточного рака лёгкого с мутацией EGFR: после терапии ингибиторами EGFR часто развивается резистентность, обусловленная амплификацией MET. В то же время биспецифические антитела EGFR×MET способны одновременно подавлять оба пути, с самого начала блокируя альтернативные механизмы выживания опухоли.
👉 Такой эффект представляет собой не простое сложение, а приводит к:
- более полной блокаде сигнальных путей
- снижению вероятности развития лекарственной устойчивости
- более длительному сохранению терапевтического эффекта
👉 По своей сути, это переход от «локального воздействия» к «системному подавлению».
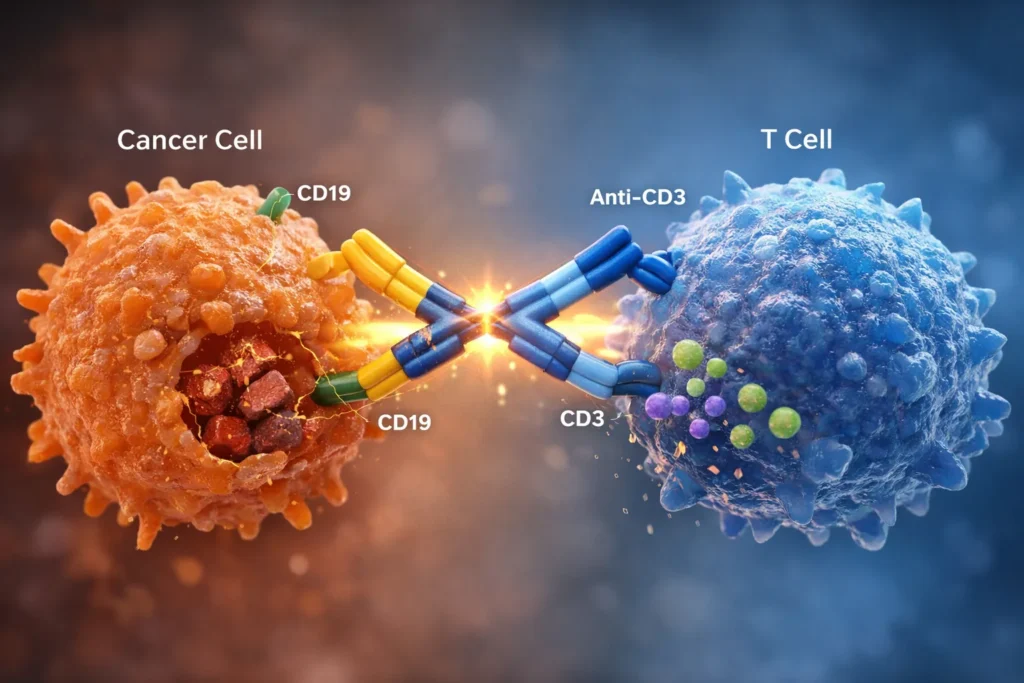
Таким образом, данный механизм формирует второй уровень логики эффекта «1+1>2»: синергия на уровне нескольких сигнальных путей → усиление контроля над сложной опухолевой системой.
(III)Двойная блокада иммунных контрольных точек: от «снятия подавления» к «полной активации»
На основе первых двух механизмов двойные специфические антитела расширяются еще на один ключевой уровень:
👉 Интегральный контроль состояния иммунной системы
Ингибиторы иммунных контрольных точек (например, антитела к PD-1/PD-L1) проявляют действие, снимая «сигналы подавления» Т-лимфоцитов, но у ингибиторов с единственной мишенью часто ограниченная частота ответа, а традиционная «комбинированная терапия двумя антителами» легко приводит к накоплению токсичности.
Двойные специфические антитела, одновременно направляясь на две иммунные контрольные точки в одной молекуле (например, PD-1×CTLA-4), обеспечивают:
- Двойное снятие иммунного подавления
- Более сильную активацию Т-лимфоцитов
- Более длительную противоопухолевую иммунную реакцию
В то же время, по сравнению с комбинированной терапией, они обладают следующими преимуществами:
- Точность выше: преимущественно проявляют действие в опухолевой микросреде
- Безопасность выше: снижают риск чрезмерной системной активации иммунитета
- Продолжительность эффективности выше: способствуют формированию иммунной памяти
На примере кадонилимумаба (Cadonilimab, PD-1×CTLA-4) можно видеть, что эта стратегия уже показала хорошие перспективы в лечении солидных опухолей.
👉 Этот механизм отражает третий уровень логики эффекта «1+1>2»: системная синергия иммунoregуляции.
✨ Эти три механизма постепенно расширяются от «локального воздействия» до «интегрального контроля», совместно формируя многоуровневую синергетическую противоопухолевую систему.
Итог основных преимуществ: от прорыва в эффективности к повышению клинической ценности
Тот факт, что двойные специфические антитела стали «ключевой технологией следующего поколения» в лечении опухолей, по своей сути обусловлено тем, что они реализовали три основных преимущества благодаря структурным инновациям, полностью переосмыслив модель лечения опухолей.
(1)Синергетичность эффективности: реализация многоуровневого объемного воздействия
Три основных механизма могут гибко комбинироваться в зависимости от типа опухоли, воздействуя на опухоль на таких уровнях, как активация иммунитета, блокада сигнала и высвобождение иммунной функции, и формируя систему «объемного боя».
Для рецидивирующих и лекарственно устойчивых опухолей этот синергетический эффект может значительно повысить частоту ремиссии, открывая новые перспективы выживания для пациентов, не реагирующих на традиционные методы лечения.
(2)Специфичность к мишеням: снижение токсических побочных эффектов лечения
Эффективность биспецифических антител основана на принципе «двойного связывания»: они проявляют активность только при одновременном распознавании опухолевых клеток и целевых мишеней (иммунных клеток или сигнальных узлов).
Это позволяет значительно снизить неспецифическое повреждение здоровых тканей, преодолеть ключевую проблему традиционной противоопухолевой терапии — сочетание эффективности и токсичности, а также существенно повысить переносимость лечения и качество жизни пациентов.
(3)Покорение лекарственной устойчивости: прорыв через ограничения традиционного лечения
Благодаря синергетическому действию на несколько мишеней, двойные специфические антитела могут полностью охватить ключевые этапы возникновения опухоли, эффективно блокировать пути избегания опухолевыми клетками уничтожения и развитие лекарственной устойчивости, продлевать долгосрочные преимущества в выживании пациентов и создать возможности для хронического управления опухолью.
👉 Именно эти преимущества позволяют двойным специфическим антителам демонстрировать ценность, превосходящую традиционные моноклональные антитела в клинической практике, и обеспечивать ядровую поддержку для «эпохи точной медицины».
Коммерциализация: поддержка цепочки поставок и соответствия требованиям для внедрения передовых методов терапии
С развитием технологии биспецифических антител (BsAb, Bispecific Antibodies) в мире уже одобрено около 20 препаратов, а сотни находятся на стадии клинической разработки. Они охватывают гематологические и солидные опухоли, аутоиммунные заболевания и другие показания, при этом глобальный рынок демонстрирует устойчивый рост.
Для зарубежных фармацевтических закупщиков освоение данного рынка требует не только понимания клинической ценности биспецифических антител, но и строгого соблюдения требований трансграничных закупок и обеспечения надежности цепочки поставок — ключевых факторов успешного внедрения передовых методов терапии.
1️⃣ Соответствие требованиям
- Проверка квалификации поставщиков и наличия международных регистраций (FDA, EMA, CDE и др.)
- Соблюдение нормативных требований на всех этапах закупки
- Консультационная поддержка по международным стандартам
2️⃣ Управление цепочкой поставок
- Специализированная логистика с контролем температуры (cold chain)
- Мониторинг в режиме реального времени при транспортировке и хранении
- Системы предупреждения и реагирования на отклонения
3️⃣ Полный цикл поставки
- Комплексные решения «под ключ»: от выбора препарата до доставки
- Поддержка логистики, таможенного оформления и документооборота
- Обеспечение быстрого доступа к инновационным препаратам
DengYueMed, обладая опытом в сфере трансграничных фармацевтических услуг, выступает надежным партнером для зарубежных закупщиков, способствуя внедрению передовых терапий и формированию полного цикла:«научные разработки → клиническая ценность → коммерческое применение».
Заключение
Биспецифические антитела, основанные на «двухмишеневой» структуре, благодаря трём ключевым механизмам — клеточному мостикованию, двойной блокаде сигнальных путей и двойной блокаде иммунных контрольных точек — обеспечили трансформацию терапевтической модели от «одиночного воздействия» к «синергетическому уничтожению», действительно реализовав противоопухолевый эффект «1+1>2».
Их ключевые преимущества заключаются в синергии эффективности, высокой точности таргетирования и способности преодолевать лекарственную устойчивость, что позволяет преодолеть ограничения традиционных моноклональных антител и делает их ключевым направлением развития онкологической терапии в эпоху прецизионной медицины.
С дальнейшим развитием технологий и углублением клинического применения показания для биспецифических антител будут продолжать расширяться, а глобальный рынок — демонстрировать устойчивый рост.
Для зарубежных фармацевтических закупщиков успешное внедрение передовых методов терапии невозможно без поддержки профессиональных решений в области цепочки поставок и соблюдения нормативных требований.
DengYue, опираясь на профессиональную экспертизу в сфере трансграничных фармацевтических услуг, способствует глобальному распространению инновационных методов лечения, включая биспецифические антитела, продвигая доступность качественных медицинских ресурсов и открывая новые возможности терапии для онкологических пациентов по всему миру.
FAQ: Биспецифические антитела и синергетический эффект
Что такое биспецифические антитела?
Биспецифические антитела (BsAb) – принципиально новое достижение в иммунотерапии рака. Это новый таргетный подход к удалению раковых клеток путем одновременного взаимодействия двух различных антигенов.
В чём основное преимущество биспецифических антител перед CAR T-клетками?
Биспецифические антитела в контексте CAR T-клеточной терапии
Терапия CAR T-клетками привлекательна тем, что это однократное лечение. Однако критическим преимуществом биспецифических антител является их доступность «сразу после покупки» , что исключает любые опасения по поводу длительных сроков обработки и потенциальных производственных сбоев.
Можно ли использовать биспецифические антитела для лечения аутоиммунных заболеваний?
Биспецифические антитела (бАт), обладающие специфичностью связывания с двумя различными целевыми молекулами, были недавно разработаны для лечения ряда аутоиммунных заболеваний , таких как ревматоидный артрит, системная красная волчанка и псориаз, и протестированы в клинических испытаниях.
Какое аутоиммунное заболевание вызывает сильную усталость?
Сильная и изнуряющая усталость — наиболее распространенная жалоба среди людей с аутоиммунными заболеваниями, такими как системная красная волчанка, рассеянный склероз, сахарный диабет 1 типа, целиакия, синдром хронической усталости и ревматоидный артрит .
