В традиционной клинической практике широко применяется стандартный подход, при котором одно и то же заболевание лечится одним и тем же препаратом в одинаковой дозировке. Однако в реальной клинической практике эффективность терапии у пациентов может существенно различаться: у одних пациентов лечение оказывается неэффективным, у других — сопровождается развитием серьезных побочных эффектов.
Основная причина заключается в индивидуальных различиях — уровне экспрессии генов, особенностях белковых структур, состоянии иммунной системы и факторах окружающей среды. В результате стандартизированные схемы лечения не всегда способны обеспечить оптимальный терапевтический эффект для каждого пациента.
Именно этим объясняется стремительное развитие персонализированной (точной) медицины — современного подхода, который предполагает отказ от модели «одно лечение для всех» и разработку индивидуальных терапевтических стратегий на основе биологических характеристик пациента, с целью повышения эффективности и безопасности лечения.
Ключевую роль в развитии персонализированной медицины играют 4 ключевых механизма лекарств в персонализированной медицине: таргетная терапия, иммунотерапия, антитело-конъюгированные препараты (ADC), а также генные и РНК-препараты.
Эти направления отличаются по механизмам действия и областям применения, охватывают ключевые потребности современной медицины и во многом определяют вектор глобального фармацевтического инновационного развития.В данной статье представлен системный обзор указанных механизмов с акцентом на их молекулярные основы, клиническое применение и примеры препаратов.
Как компания, специализирующаяся на поставке лекарственных средств и работе с инновационными препаратами, HongKong DengYue Medicine внимательно отслеживает развитие передовых терапевтических технологий и стремится обеспечивать рынок качественными лекарственными решениями и профессиональной информационной поддержкой.
Таргетная терапия: специфическая терапия на основе молекулярных мишеней
Традиционные цитотоксические химиопрепараты действуют на процесс клеточной пролиферации, не обладая избирательностью между быстро делящимися здоровыми и патологическими клетками, что часто вызывает побочные эффекты со стороны многих систем организма.
👉 Таргетная терапия направлена на специфические молекулярные маркеры патологических клеток. Путем специфического связывания препарата с мишенью она блокирует сигнальные пути, отвечающие за пролиферацию и метастазирование патологических клеток, или индуцирует их апоптоз, минимизируя повреждение здоровых тканей и повышая безопасность и точность лечения.
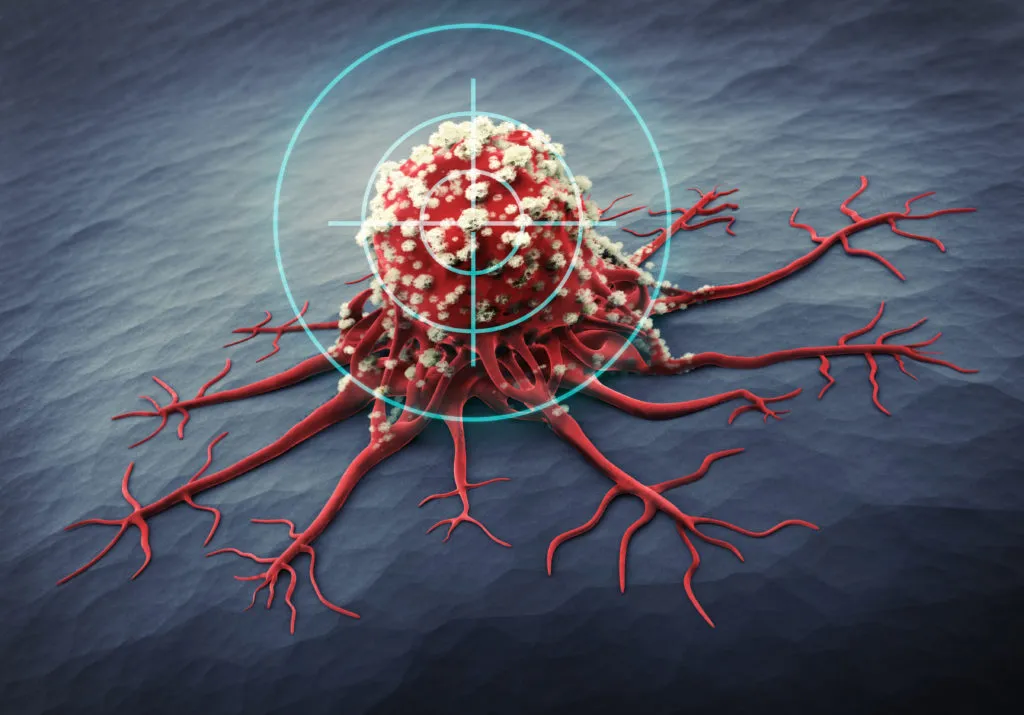
Основной принцип действия таких препаратов — воздействие на специфические мишени (мутированные гены, аномально экспрессированные белки, нарушенные сигнальные пути) и эффект только на патологические клетки, содержащие соответствующую мишень.
Именно это делает таргетную терапию основным механизмом персонализированной медицины.
Основные области применения + типичные примеры препаратов
Таргетная терапия является наиболее зрелым и широко применяемым методом персонализированного лечения в области злокачественных опухолей, охватывая большинство распространенных видов рака. Постепенно она расширяется и на другие области: аутоиммунные заболевания, хронические метаболические заболевания и др. Основные клинические сценарии применения:
- Немелкоклеточный рак легкого:
- Kак эталонная область таргетной терапии. Для пациентов с чувствительными мутациями EGFR применяются препараты гефитиниб, осимертиниб; для пациентов с слиянием гена ALK — кризотиниб, церитиниб.
- После скрининга мишени с помощью генетического теста эффективность лечения значительно выше, чем при традиционной химиотерапии.
- Рак молочной железы:
- У пациентов с HER2-положительным раком молочной железы применение трастузумаба (Герцептин) для таргетной блокировки пути белка HER2 снижает риск рецидива заболевания;
- У пациентов с HR-положительным раком молочной железы — пальбоциклиб для ингибирования клеточного цикла и замедления прогрессирования опухоли.
- Лейкоз
- Xронический миелоидный лейкоз вызван аномальной экспрессией слияния генов BCR-ABL. Классический таргетный препарат иматиниб (Гливек) специфически ингибирует активность продукта этого слияния, превращая смертельное заболевание в хроническую патологию, поддающуюся длительному контролю, и значительно улучшая выживаемость пациентов.
- Аутоиммунные заболевания:
- У пациентов с ревматоидным артритом, анкилозирующим спондилитом применение адалимумаба для ингибирования воспалительного фактора TNF-α снимает воспалительное повреждение суставов;
- У пациентов с псориазом — секьюкинаб для блокировки пути IL-17A и контроля аномальной пролиферации кожи.
🤔 Важное клиническое замечание: предпосылкой применения таргетной терапии является подтверждение наличия соответствующей терапевтической мишени в организме пациента.
В клинической практике для этого используются методы сопутствующей диагностики:
- генетическое тестирование
- иммуногистохимия
- молекулярное профилирование
👉 Только пациенты с подтверждённой мишенью получают значимую пользу от терапии, что является ключевым принципом персонализированной медицины.
Таргетная терапия обеспечивает точное воздействие на патологические клетки и устраняет недостаток избирательности традиционной химиотерапии, но у части пациентов развивается резистентность к мишеням. Чтобы преодолеть эти ограничения и активировать собственную защитную силу организма, иммунотерапия как другой ключевой механизм стала важным дополнением персонализированной медицины.
Иммунотерапия: противоопухолевая терапия, регулирующая иммунную систему организма
Иммунная система организма обладает физиологической функцией распознавания и уничтожения аномальных клеток. Однако опухолевые клетки могут уклоняться от надзора иммунной системы различными механизмами — это явление называется иммунным уклонением, и оно является важным механизмом развития злокачественных опухолей.
👉 Иммунотерапия не оказывает прямого цитотоксического действия на опухолевые клетки, а регулирует активность иммунных клеток организма с помощью препаратов, снимает иммунное подавление, опосредованное опухолевыми клетками, и восстанавливает способность иммунных клеток распознавать и уничтожать опухолевые клетки.
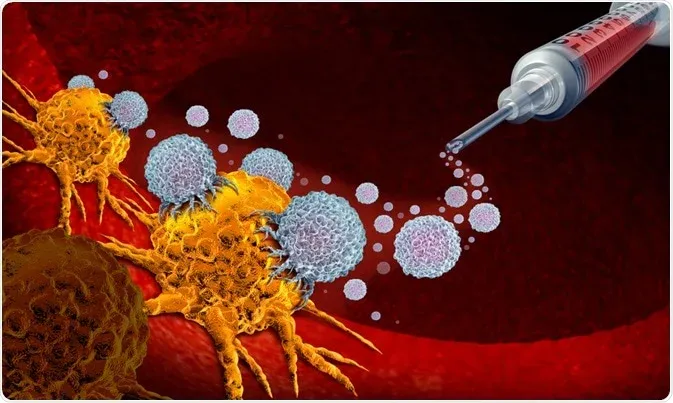
По сравнению с другими механизмами терапии, иммунотерапия за счет памяти иммунной системы обеспечивает длительный противоопухолевой эффект и снижает риск рецидива заболевания — это преимущество делает ее перспективным методом в персонализированной медицине.
Основные области применения + типичные примеры препаратов
Основная область применения иммунотерапии — злокачественные опухоли, она обладает широким противоопухолевым действием, не ограниченным одним видом рака. Постепенно она используется для регуляции иммунитета при аутоиммунных и инфекционных заболеваниях. Клинически выделяют два основных типа:
1. Ингибиторы иммунных контрольных точек (наиболее широко применяются в клинике)
- Ингибиторы PD-1: пембролизумаб (Препарат К), ниволумаб (Препарат О),синтилизумаб и др. Одобрены для лечения десятков солидных и гематологических опухолей: рак легкого, меланома, рак печени, рак желудка, рак шейки матки и др. Чем выше уровень экспрессии PD-L1 и нагрузка мутаций опухоли (TMB) у пациента, тем выше вероятность пользы от терапии.
- Ингибиторы CTLA-4: ипилимумаб, часто применяется в комбинации с ингибиторами PD-1 для лечения трудноподдающихся терапии опухолей: меланома, рак почки и др., повышая ответ на противоопухолевую терапию.
2. Адоптивная клеточная терапия
Представительным методом является CAR-T-клеточная терапия: из собственных Т-клеток пациента в лаборатории создают генетически модифицированные клетки, экспрессирующие рецептор к опухолевому антигену, после размножения их вводят обратно пациенту для специфического уничтожения опухолевых клеток.
- Классические препараты — акилтенсе, реджиотенсе, применяются для лечения рецидивирующего и рефрактерного лейкоза, лимфомы, множественной миеломы, давая шанс на выздоровление поздним пациентам.
➡️ Важное клиническое замечание: иммунотерапия действует за счет активации иммунной системы организма, поэтому может вызывать иммуноопосредованные побочные эффекты:нарушение функции щитовидной железы, иммунный пневмонит, энтерит и др. Эти побочные эффекты в большинстве случаев контролируются клиническими вмешательствами, а общая переносимость лучше, чем при традиционной химиотерапии.
Иммунотерапия обеспечивает длительный противоопухолевой эффект за счет иммунной системы организма, но при резистентных опухолях с четкими мишенями и высокой потребностью в цитотоксичности моноиммунотерапия имеет ограниченную эффективность.
Препараты-АДК, сочетающие точность таргетного воздействия и цитотоксический эффект, стали ключевым инновационным механизмом для преодоления резистентности и усиления терапевтического эффекта.🔻
Препараты-АДК: таргетная цитотоксическая терапия, опосредованная антитело-конъюгацией
Антитело-конъюгаты (АДК) — инновационные препараты, объединяющие технологию моноклональных антител и цитотоксических средств. Они состоят из трех частей: моноклональное антитело, линкер и груз цитотоксического препарата.
Механизм их действия делится на три этапа:
- Во-первых, моноклональное антитело специфически распознает антиген на поверхности опухолевой клетки, обеспечивая таргетное накопление препарата в области опухоли;
- Во-вторых, линкер сохраняет стабильную структуру в кровотоке, предотвращая преждевременное высвобождение цитотоксического препарата, и специфически расщепляется после поглощения АДК опухолевой клеткой;
- Наконец, высвобожденный цитотоксический препарат действует внутри опухолевой клетки, индуцируя ее апоптоз, а также убивает соседние опухолевые клетки за счет «эффекта зрителя», повышая общий цитотоксический эффект.
Основные области применения + типичные примеры препаратов
Препараты-АДК предназначены в основном для поздних злокачественных опухолей с четкими мишенями и резистентностью к традиционной терапии, являются улучшенной формой таргетной терапии и эффективно заполняют пробел в лечении после развития резистентности к таргетным препаратам. Основные клинические применения:
- HER2-положительный рак молочной железы/желудка:
- Трастузумаб эмтанзин (T-DM1), Трастузумаб дерукстекан (T-DXd). Для пациентов с гиперэкспрессией HER2 даже при резистентности к трастузумабу они значительно продлевают безрецидивную и общую выживаемость.
- Тройной негативный рак молочной железы:
- Сацитузумаб говитекан, таргетирующий мишень Trop-2, заполняет пробел в отсутствии эффективных таргетных препаратов для этого вида рака и повышает эффективность лечения поздних пациентов.
- Рак мочевыводящих путей, рак легкого:
- Диситамаб ведотин (отечественный ADC), Сацитузумаб говитекан
применяются у пациентов с резистентными формами заболевания, обеспечивая более высокую эффективность по сравнению с традиционной химиотерапией.
- Диситамаб ведотин (отечественный ADC), Сацитузумаб говитекан
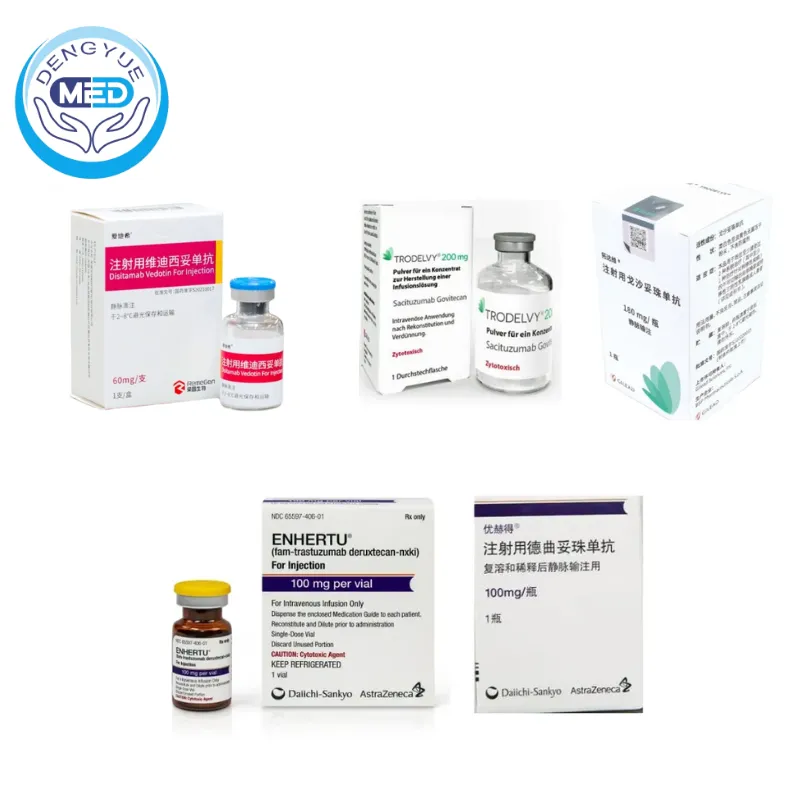
✨ Клинические преимущества: по сравнению с монотаргетными препаратами АДК обладают более сильной цитотоксичностью и эффективно преодолевают опухолевую резистентность; по сравнению с традиционной химиотерапией их свойство таргетного накопления снижает системные токсические реакции, сочетая эффективность и безопасность лечения. Это ключевое направление точной терапии поздних опухолей.
Препараты-АДК сочетают таргетность и цитотоксичность, решая проблему лечения резистентных солидных опухолей, но при генетических заболеваниях, вызванных дефектами генов, существующие препараты только снимают симптомы, не обеспечивая радикального излечения.
Генные/РНК-препараты: радикальная терапия, направленная на генетический материал
Большинство редких генетических заболеваний, некоторые злокачественные опухоли и инфекционные болезни вызваны дефектами, мутациями или аномальной экспрессией генов, что приводит к нарушению синтеза функциональных белков или образованию токсичных белков в организме. Традиционные препараты только снимают симптомы заболевания, не устраняя нарушения на уровне генетического материала.
👉 Генные/РНК-препараты действуют непосредственно на уровне генов или РНК: путем восстановления дефектных генов, замены нормальными генами, блокировки трансляции патогенной РНК и др. Они регулируют экспрессию белков изнутри, обеспечивая радикальное излечение или длительную ремиссию заболевания, охватывая «недоступные для лекарств мишени», на которые не действуют традиционные препараты.
Такие препараты делятся на две основные категории: генная терапия и РНК-препараты. Оба типа являются передовыми технологиями персонализированной медицины.
Основные области применения + типичные примеры препаратов
Генные/РНК-препараты применяются в основном в трех областях: редкие генетические заболевания, злокачественные опухоли и инфекционные заболевания, преодолевая терапевтический тупик многих сложных болезней. Основные клинические сценарии:
1. Редкие генетические заболевания (основная область применения)
- Спинальная мышечная атрофия (SMA):
- Нусинерсен корректирует сплайсинг РНК при интратекальном введении;
- Zolgensma обеспечивает доставку функционального гена SMN1 после однократного введения.
- Гемофилия:
- Эмицизумаб, а также генные препараты на основе AAV-векторов позволяют компенсировать дефицит факторов свертывания крови и снизить зависимость от регулярных трансфузий.
- Наследственный транстиретиновый амилоидоз:
- Патисиран подавляет синтез патологического белка за счёт деградации соответствующей РНК.
2. Инфекционные заболевания
Успешным примером в этой области являются мРНК-вакцины, например вакцины от COVID-19.
Они поставляют мРНК, которая направляет организм на синтез специфического антигена и активирует адаптивный иммунный ответ. Обладают коротким циклом разработки и высокой гибкостью, в будущем могут быть адаптированы для создания вакцин от гриппа, ВИЧ и других инфекционных заболеваний.
3. Злокачественные опухоли
СиРНК-препараты, направленные на драйверные гены опухоли, и терапия редактирования генов CRISPR-Cas9 находятся на стадии клинических испытаний. Они уничтожают онкогены, восстанавливают опухолевые супрессорные гены, подавляют пролиферацию опухолевых клеток изнутри и открывают новый путь лечения поздних рефрактерных опухолей.
Генные/РНК-препараты обеспечивают переход от «симптоматической терапии» к «радикальному излечению», что знаменует переход персонализированной медицины на новый этап.
Четыре лекарственных механизма имеют разные акценты и дополняют друг друга, совместно формируя целостную систему терапии персонализированной медицины и определяя основные направления развития фармацевтической отрасли в будущем.
Совместное развитие четырех механизмов: будущее персонализированной медицины
Таргетная терапия, иммунотерапия, антитело-конъюгированные препараты (ADC) и генные и РНК-препараты не существуют изолированно, а формируют взаимодополняющую терапевтическую систему. Их совместное развитие способствует трансформации персонализированной медицины из высокотехнологичной ниши в более доступную модель здравоохранения.
В ближайшие годы развитие фармацевтической отрасли будет сосредоточено на следующих ключевых направлениях:
1. Комбинированная терапия станет клиническим стандартом для преодоления опухолевой резистентности
Развитие лекарственной резистентности при монотерапии остаётся одной из ключевых проблем современной медицины.
👉 В клинической практике всё большее значение будут приобретать комбинированные схемы лечения:
- таргетная терапия + ингибиторы иммунных контрольных точек
- ADC + иммунотерапия
- генная терапия + клеточная терапия
📌 Такие подходы позволяют сочетать точечное воздействие, цитотоксический эффект и длительный иммунный ответ, замедляя развитие резистентности и увеличивая число пациентов, получающих клиническую пользу.
2. Технологические инновации снизят стоимость лечения и преодолеют барьер высоких цен
В настоящее время инновационные препараты, такие как ADC и генные/РНК-терапии, остаются дорогостоящими и ограниченно доступными.
👉 В будущем ожидается:
- оптимизация технологий линкеров и систем доставки (например, AAV, LNP)
- развитие масштабируемого производства
- снижение затрат на разработку и производство
📌 Одновременно расширение применения сопутствующей диагностики и повышение охвата медицинским страхованием будут способствовать более широкому доступу пациентов к современным методам лечения.
3. Расширение показаний к применению: охват всех групп заболеваний
4 ключевых механизма лекарств в персонализированной медицине постепенно выйдут за рамки онкологии и расширятся на области хронических метаболических заболеваний, нейродегенеративных заболеваний, коррекции старения и др.
👉 Например, РНК-препараты для длительного контроля гиперлипидемии и артериальной гипертензии, таргетные препараты для нейропротекции при болезни Альцгеймера, иммунотерапия для точного регулирования аутоиммунных заболеваний — это обеспечит переход от лечения тяжелых болезней к полноцикловому управлению здоровьем.
4. Глубокое внедрение ИИ: повышение точности диагностики и лечения
Искусственный интеллект будет интегрирован во все процессы: разработка лекарств, скрининг мишеней, стратификация пациентов, подбор схем лечения.
- Алгоритмы ИИ быстро выявят новые мишени, оптимизируют молекулярную структуру препаратов и сократят цикл разработки.
- Анализ мультиомических данных (геном, протеом, метаболом) с помощью ИИ обеспечит точный подбор пациентов и терапевтических схем, реализуя идею персонализированной медицины «один пациент — одна схема лечения».
Заключение
Развитие персонализированной медицины представляет собой непрерывный процесс повышения точности диагностики и лечения.
Таргетная терапия обеспечивает селективное воздействие на патологические клетки, иммунотерапия активирует собственные защитные механизмы организма, антитело-конъюгированные препараты (ADC) объединяют таргетность и цитотоксический эффект, а генные и РНК-препараты воздействуют непосредственно на генетическую основу заболевания.
👉 В совокупности эти подходы формируют 4 ключевых механизма лекарств в персонализированной медицине, которые лежат в основе современной терапевтической стратегии и взаимно дополняют друг друга.
По мере дальнейшего развития технологий и совершенствования медицинской экосистемы персонализированная медицина будет становиться всё более доступной и постепенно перейдёт в категорию стандартной клинической практики, обеспечивая более точную диагностику, безопасную фармакотерапию и более высокие шансы на успешное лечение.
FAQ: 4 ключевых механизма лекарств в персонализированной медицине
Что значит персонализированная медицина?
Персонализированная медицина представляет собой современный подход в здравоохранении, который учитывает индивидуальные особенности каждого пациента для оптимизации диагностики, лечения и профилактики заболеваний.
Каковы 4 принципа персонализированной медицины?
Четыре «П» персонализированной медицины — это прогнозирование, профилактика, персонализация и участие .
Этот подход использует передовые технологии, такие как геномика и большие данные.
Четыре «П» представляют собой новую парадигму в здравоохранении, ориентированную на профилактику и персонализацию.
Что такое персонализация лечения?
Персонализированная или точная медицина — это парадигма, при которой врач учитывает уникальные генетические, экологические и образ жизни факторы пациента для разработки оптимальной стратегии диагностики и лечения.
Главные тренды современной медицины?
Медицина будущего: 7 главных трендов
1. Интернет вещей для медицины (IoT)
2. Мобильные приложения, оказывающие медицинскую поддержку, или mhealth.
3. Искусственный интеллект (ИИ) в медицине
4. Технология редактирования генома
5. Телемедицина
6. Внедрение блокчейна в медицине
7.Биохакинг
